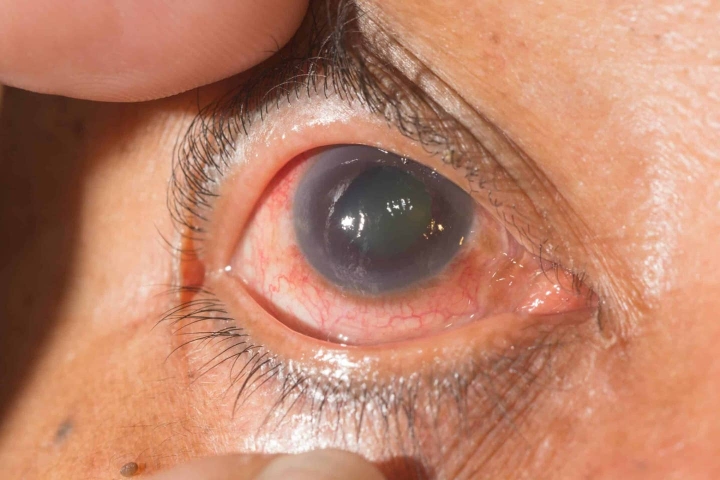
Инновационное исследование использует искусственный интеллект для выявления HG9-91-01, потенциального средства для лечения глаукомы, которое дает надежду на нейропротекцию и сохранение зрения. (ФОТО: CC BY-SA 4.0)
Глаукома, вторая по распространенности причина слепоты во всем мире, поражает миллионы людей и, по прогнозам, к 2040 году достигнет 111,8 миллионов случаев. Это прогрессирующее заболевание глаз возникает в результате скопления жидкости, повышения внутриглазного давления (ВГД) и повреждения зрительного нерва.
Хотя существуют методы лечения, снижающие ВГД, они не останавливают прогрессирование заболевания у всех пациентов. Ганглиозные клетки сетчатки (RGC), которые передают зрительные сигналы от глаза к мозгу, часто подвергаются дегенерации, что приводит к дальнейшему повреждению зрительного нерва. Это подчеркивает настоятельную необходимость в нейропротекторных методах лечения, дополняющих методы, снижающие давление.
Недавние исследования выявили некроптоз, тип запрограммированной гибели клеток, как ключевой фактор потери RGC. Опубликованное в китайском медицинском журнале исследование «некроптоз» имеет общие характеристики с апоптозом (естественным разрушением клеток) и некрозом (повреждением клеток, связанным с травмой), а взаимодействующая с рецепторами протеинкиназа 3 (RIPK3) играет центральную роль в этом процессе.
Воздействие на RIPK3 может обеспечить новый подход к сохранению RGC и предотвращению дальнейшего повреждения. Достижения в области искусственного интеллекта (ИИ) открывают путь к прорывам в выявлении эффективных ингибиторов RIPK3, что дает надежду пациентам с острой глаукомой.
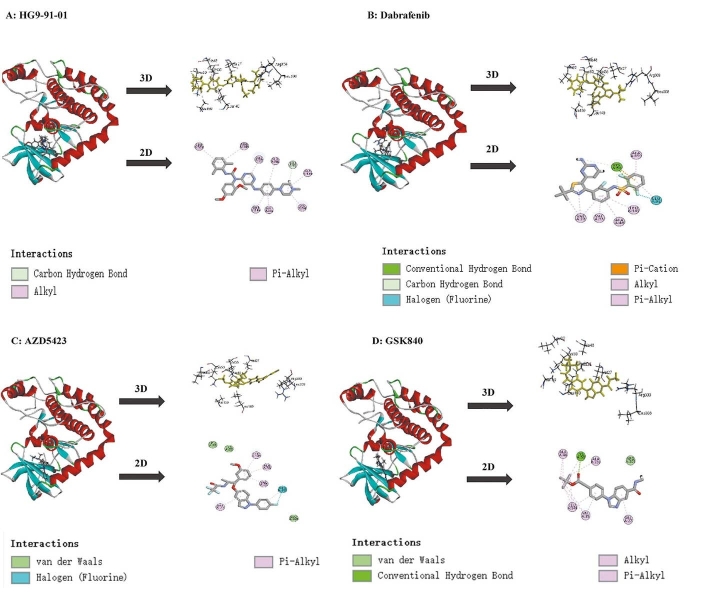
Визуализация результатов молекулярного докинга и статистического анализа остатков. (ПРЕДОСТАВЛЕНО Китайским медицинским журналом)
Искусственный интеллект произвел революцию в разработке лекарств, оптимизировав процессы и ускорив поиск потенциальных методов лечения. Исследовательская группа использовала передовые модели искусственного интеллекта, в том числе модели больших языков (LLM) и графические нейронные сети, для идентификации соединений, нацеленных на RIPK3. Их результаты показывают, как подходы, основанные на ИИ, могут помочь в разработке новых методов лечения острой глаукомы.
Используя инструменты искусственного интеллекта, такие как ChatGPT и DynamicBind, исследователи составили список низкомолекулярных соединений, которые могут взаимодействовать с RIPK3. Эти инструменты отсортировали лекарственные препараты-кандидаты на основе прогнозируемого сродства связывания, подтвержденного с помощью молекулярного моделирования и биологических экспериментов.
Доктор Юаньсу Гао, один из ведущих исследователей, отметил, что “искусственный интеллект предоставляет надежные инструменты и методы для поиска лекарств, такие как виртуальный скрининг, количественное моделирование взаимосвязи структуры и активности и разработка новых лекарств”.
Поиск лекарств традиционно был длительным и ресурсоемким процессом, на который часто уходили годы, чтобы определить жизнеспособные варианты лечения. Алгоритмы искусственного интеллекта, напротив, могут анализировать огромные массивы данных в кратчайшие сроки.
В этом исследовании ученые использовали возможности искусственного интеллекта для прогнозирования взаимодействий между малыми молекулами и RIPK3, что значительно сократило сроки скрининга лекарств. Такой подход не только ускоряет открытие, но и снижает затраты, связанные с традиционными методами разработки лекарств.
Среди выявленных кандидатов наиболее перспективным ингибитором RIPK3 оказался HG9-91-01. Молекулярное моделирование подтвердило, что HG9-91-01 образует стабильный комплекс с RIPK3, превосходя других кандидатов по сродству связывания и профилю безопасности.
Прогнозы по показателям ADMET (всасывание, распределение, метаболизм, экскреция и токсичность) также подтвердили пригодность соединения в качестве лекарственного средства.
Эффективность соединения была подтверждена в экспериментах как in vitro, так и in vivo. В лабораторных тестах, имитирующих повреждение зрительного нерва, пациенты, подвергшиеся кислородно-глюкозной депривации (ОГД), показали значительно более высокие показатели выживаемости при лечении препаратом HG9-91-01 по сравнению с другими кандидатами. Кроме того, HG9-91-01 снижал маркеры пироптоза, типа гибели клеток воспаления, демонстрируя его роль в уменьшении потери RGC.
Профессор Чжан Кан, соавтор исследования, подчеркнул инновационный подход, заявив: “Хотя многочисленные исследования были сосредоточены на антиапоптотических, некроптотических и антипироптотических препаратах для лечения острой глазной гипертензии, стратегии, нацеленные на паноптоз, упоминаются редко. В этом исследовании рассматриваются потенциальные лекарственные средства, нацеленные на RIPK3, для предотвращения гибели RGC и каскада механизмов клеточной гибели”.
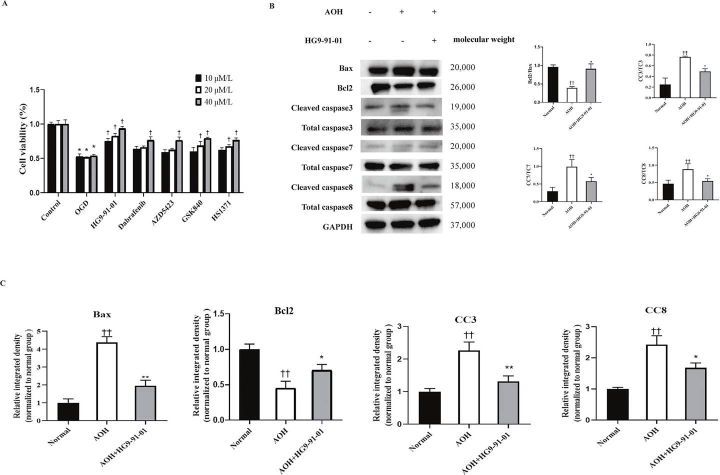
Влияние HG9-91-01 на экспрессию белков, ассоциированных с апоптозом, у мышей с AOH. (ФОТО: Китайский медицинский журнал)
Инновационное использование ИИ в этом контексте подчеркивает его преобразующий потенциал в современной медицине. Объединив вычислительные методы с традиционными лабораторными методами, исследователи достигли уровня точности и эффективности, ранее недостижимого.
Способность искусственного интеллекта прогнозировать эффективность и безопасность лекарств in silico гарантирует, что только наиболее перспективные кандидаты пройдут экспериментальную проверку, тем самым экономя ценные ресурсы.
В мышиных моделях острой глаукомы HG9-91-01 проявлял нейропротекторные эффекты, сохраняя структуру сетчатки и предотвращая ее истончение — распространенное следствие повышенного ВГД. Соединение ингибировало активацию сигнальных молекул, связанных с апоптозом, пироптозом и некроптозом, которые в совокупности называются паноптозом. Регулируя эти пути, HG9-91-01 продемонстрировал свой потенциал в защите сетчатки и сохранении зрительных функций.
Истончение сетчатки, являющееся признаком прогрессирования глаукомы, напрямую связано с потерей остроты зрения. Способность HG9-91-01 поддерживать толщину сетчатки позволяет предположить, что он может замедлять или даже останавливать дегенеративные процессы, лежащие в основе глаукомы.
Кроме того, его роль в подавлении паноптоза подчеркивает его потенциал как многоцелевого терапевтического средства. В отличие от методов лечения, которые направлены исключительно на снижение ВГД, HG9-91-01 устраняет первопричины потери RGC, предлагая более комплексное решение.
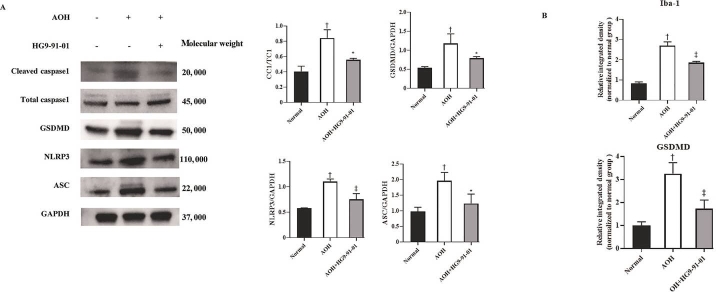
Влияние HG9-91-01 на экспрессию белков, ассоциированных с пироптозом, у мышей с AOH. (ФОТО: Китайский медицинский журнал)
Дальнейший анализ показал, что HG9-91-01 регулирует ключевые белки, участвующие в процессах гибели клеток, снижая экспрессию маркеров, связанных с апоптозом, пироптозом и некроптозом. Эти результаты дают ценную информацию о молекулярных механизмах, лежащих в основе его нейропротекторных эффектов. Благодаря одновременному воздействию на несколько путей, HG9-91-01 представляет собой значительный прогресс в лечении нейродегенеративных заболеваний глаз.
Исследование подчеркивает преобразующий потенциал ИИ в разработке лекарств. Сочетая вычислительные инструменты с биологической проверкой, исследователи могут ускорить поиск эффективных методов лечения. Однако для обеспечения этичного и надежного применения ИИ в медицине необходимо решить такие проблемы, как конфиденциальность данных, прозрачность и предвзятость.
Доктор Гао подчеркнул важность дальнейших исследований, заявив: “Технологии искусственного интеллекта полезны для решения задач, требующих больших вычислительных затрат, и принятия рациональных решений на основе сложных мультимодальных знаний. Однако необходимы дальнейшие подтверждающие исследования сетчатки, чтобы подтвердить эффективность HG9-91-01 в защите структуры сетчатки у пациентов с острой глазной гипертензией”.
Результаты этого исследования выходят за рамки глаукомы и демонстрируют потенциал методов, основанных на искусственном интеллекте, для лечения других нейродегенеративных заболеваний. Совершенствуя эти методы, ученые могут разрабатывать целевые методы лечения широкого спектра заболеваний, от болезни Альцгеймера до болезни Паркинсона. Интеграция ИИ в биомедицинские исследования знаменует собой новую эру инноваций, когда подходы, основанные на данных, дополняют традиционные научные методы.
По мере того, как исследователи совершенствуют методы создания лекарств, основанные на ИИ, будущее лечения глаукомы выглядит более радужным. Определение HG9-91-01 в качестве потенциального средства для лечения является примером того, как передовые технологии и научная изобретательность могут решать неотложные медицинские задачи. Используя возможности искусственного интеллекта, ученые не только ускоряют разработку лекарств, но и улучшают перспективы пациентов, подверженных риску потери зрения.
Более того, совместный характер этого исследования подчеркивает важность междисциплинарных усилий в развитии медицинской науки. Объединив экспертов в области искусственного интеллекта, фармакологии и офтальмологии, команда продемонстрировала, как различные точки зрения могут привести к революционным открытиям. Этот подход создает прецедент для будущих исследований, подчеркивая ценность сотрудничества в решении сложных проблем здравоохранения.
Поскольку глобальное бремя глаукомы продолжает расти, потребность в инновационных методах лечения становится все более насущной. Прорывы, основанные на ИИ, такие как HG9-91-01, позволяют заглянуть в будущее, в котором потеря зрения, возможно, больше не будет неизбежным исходом для миллионов пациентов.
Благодаря постоянным исследованиям и сотрудничеству мечта о предотвращении слепоты становится все более достижимой.